安罗替尼治疗非小细胞肺癌患者对其肿瘤标志物表达的影响作用研究
黄 浩
(惠东县人民医院肿瘤科,广东惠州 516300)
非小细胞肺癌属于肺癌的病理类型之一,在临床中较为常见,其在发病早期多无明显症状,但随着病情的加重,患者可逐渐出现咳嗽、胸痛等症状,且在临床确诊时病情多已发展至晚期,进而可使得其预后较差,缩短生命周期[1]。现阶段,常规单药化疗是临床治疗非小细胞肺癌常采用的方案之一,其主要是根据患者耐受情况,予以单药化疗药物治疗,虽可缓解患者的临床症状,延长其生命时间,但其在临床应用中部分患者易发生疲劳、蛋白尿等不良反应[2]。安罗替尼是一种新型制剂,其可通过多靶点对酪氨酸激酶发挥抑制作用,从而达到避免病情恶化的目的,临床常用于复发转移性食管鳞癌、晚期肝癌德等疾病患者的治疗中,且现已取得了良好的临床效果[3]。基于此,本研究旨在探讨安罗替尼治疗非小细胞肺癌患者对其肿瘤标志物表达的影响,以便临床寻找出更有效的治疗方案,现将结果报道如下。
1.1 一般资料 选取2018年4月至2021年4月惠东县人民医院收治的112例患者,按随机数字表法分为对照组和试验组,各56例。对照组患者中男性35例,女性21例;
年龄50~78岁,平均年龄(62.68±5.56)岁;
病程6个月~3年,平均病程(2.15±0.48)年;
分期:Ⅲb期32例,Ⅳ期24例。试验组患者中男性34例,女性22例;
年龄50~79岁,平均年龄(62.52±5.67)岁;
病程7个月~3年,平均病程(2.24±0.52)年;
分期:Ⅲb期33例,Ⅳ期23例。两组患者一般资料比较,差异无统计学意义(P>0.05),可进一步对比其他指标。本研究经惠东县人民医院医学伦理委员会批准。患者及其家属知情并签署知情同意书。纳入标准:①此次研究以《非小细胞肺癌诊疗指南:循证医学与治疗学基础》[4]为诊断依据,且所有患者均经病理学检查确诊;
②伴有咳嗽、胸痛等症状者;
③能自行或在他人帮助下配合研究者;
④身体因晚期化疗周期数较多而不能耐受联合化疗者;
⑤经二线及以上治疗后,病情复发或有进展者。排除标准:①凝血功能异常者;
②合并其他组织器官严重疾病者;
③对本研究所使用药物感到强烈不适且无法缓解者;
④中央型鳞癌,伴有空洞者。
1.2 治疗方法 将常规化疗予以对照组:静脉注射盐酸吉西他滨(哈药集团生物工程有限公司,国药准字H20113397,规格:0.2 g),1 000 mg/m2,注射时间控制为30 min;
长春瑞滨(长春雷允上药业有限公司,国药准字H20041927,规格:10 mg)25 mg/m2,注射时间控制在15~20 min以内,21 d为1个疗程,期间给予止吐、抗感染治疗。予以试验组患者口服盐酸安罗替尼胶囊(正大天晴药业集团股份有限公司,国药准字H20180002,规格:12 mg)治疗,12 mg/次,1次/d,连续应用14 d,停药7 d,再循环用药。两组均以21 d为1个疗程,连续治疗3个疗程。
1.3 观察指标 ①对比临床疗效。治疗后,使用《实体瘤治疗疗效评价标准-RECIST》[5]进行评估,其中完全缓解(CR):治疗后,患者病灶完全消失,且时间持续28 d;
部分缓解(PR):治疗后,患者肿瘤最大垂直直径、最大直径的总和缩短50%及以上,且时间持续28 d;
稳定(SD):治疗后,患者肿瘤最大垂直直径、最大直径的总和缩短50%以下,或增长25%及以下,且无新病灶,时间持续28 d;
进展(PD)治疗后,患者肿瘤最大垂直直径、最大直径的总和增长25%以上,且伴随新病灶出现。临床疾病控制率(DCR)=1-PD率。②对比血清血管内皮生长因子(VGEF)、癌胚抗原(CEA)、细胞角蛋白19片段抗原21-1(CYFRA21-1)水平。治疗前后,抽取两组患者空腹外周静脉血约5 mL,待其凝固后,离心分离血清(离心条件:3 000 r/min、10 min),使用全自动生化分析仪(天津诺迈科技有限公司,型号:LOC-200)、酶联免疫吸附法测定血清VGEF水平,使用电化学发光免疫分析法测定血清CEA、CYFRA21-1水平。③两组患者治疗前后生活质量比较。治疗前后,使用肺癌患者生活质量量表(QLQ-LC13)[6]评分进行评估两组患者的生活质量,其中QLQ-LC13评分主要包括咳嗽、气促、口腔疼痛、手足刺痛、脱发、胸痛、吞咽困难等内容,每项评分0~100分,患者最终得分与其生活质量呈负相关。④两组患者治疗期间不良反应比较。治疗期间,统计两组患者高血压、肝或肾功能障碍、甲状腺功能障碍、口腔黏膜炎、蛋白尿、疲劳等不良反应发生情况。不良反应发生率=不良反应发生例数/总例数×100%。
1.4 统计学分析 采用SPSS 27.0统计学软件对数据进行分析。计数资料以[例(%)]表示,采用χ2检验;
计量资料以(±s)表示,采用t检验。P<0.05表示差异有统计学意义。
2.1 两组患者治疗后临床疗效比较 治疗后,试验组患者临床疾病控制率高于对照组,差异有统计学意义(P<0.05),见表1。
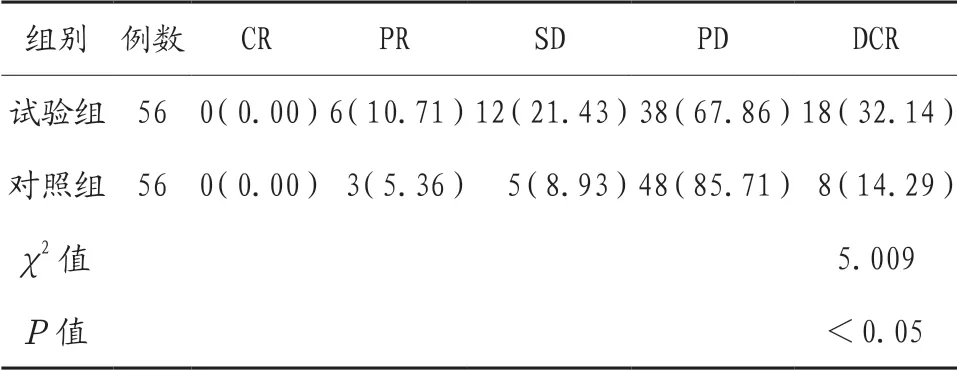
表1 两组患者治疗后临床疗效比较[例(%)]
2.2 两组患者治疗前后血清VGEF、CEA、CYFRA21-1水平比较 两组患者血清VGEF、CEA、CYFRA21-1水平治疗后与治疗前比较均降低,其中试验组与对照组相比,处于更低水平,差异均有统计学意义(均P<0.05),见表2。
表2 两组患者治疗前后血清VGEF、CEA、CYFRA21-1水平比较( ±s )

表2 两组患者治疗前后血清VGEF、CEA、CYFRA21-1水平比较( ±s )
注:与治疗前比,*P<0.05。VGEF:血管内皮生长因子;
CEA:癌胚抗原;
CYFRA21-1:细胞角蛋白19片段抗原21-1。
组别 例数 VGEF(pg/mL) CEA(ng/mL) CYFRA21-1(ng/mL)治疗前 治疗后 治疗前 治疗后 治疗前 治疗后试验组 56 286.57±31.35 196.56±23.11* 15.48±2.37 9.57±2.12* 8.52±0.87 4.48±0.50*对照组 56 285.52±32.37 251.35±25.18* 15.45±2.35 13.18±2.15* 8.48±0.89 5.95±0.64*t值 0.174 -11.996 0.067 -8.947 0.241 -13.545 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05
2.3 两组患者治疗前后生活质量比较 两组患者咳嗽、气促、口腔疼痛、手足刺痛、脱发、胸痛、吞咽困难评分治疗后与治疗前比较均降低,其中试验组与对照组相比,处于更低水平,差异均有统计学意义(均P<0.05),见表3。
表3 两组患者治疗前后生活质量比较(分,±s )

表3 两组患者治疗前后生活质量比较(分,±s )
注:与治疗前比,*P<0.05。
组别 例数 咳嗽 气促 口腔疼痛 手足刺痛治疗前 治疗后 治疗前 治疗后 治疗前 治疗后 治疗前 治疗后试验组 56 52.15±5.78 38.58±4.36* 48.53±5.46 37.71±3.27* 42.78±4.74 31.35±3.69* 36.22±3.33 29.72±3.29*对照组 56 51.67±5.85 45.17±4.62* 48.44±5.58 43.12±3.46* 41.63±4.67 36.74±3.47* 36.18±3.36 32.47±3.14*t值 0.437 -7.763 0.086 -8.504 1.293 -7.963 0.063 -4.525 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05组别 例数 脱发 胸痛 吞咽困难治疗前 治疗后 治疗前 治疗后 治疗前 治疗后试验组 56 36.87±4.67 30.55±3.65* 37.25±3.44 30.25±3.24* 36.84±3.47 31.25±3.38*对照组 56 37.18±4.35 34.18±3.18* 36.44±3.37 33.53±3.47* 37.52±3.85 34.68±3.65*t值 -0.363 -5.611 1.259 -5.170 -0.982 -5.160 P值 >0.05 <0.05 >0.05 <0.05 >0.05 <0.05
2.4 两组患者治疗期间不良反应比较 治疗期间,试验组患者发生高血压5例(8.93%),肝、肾功能障碍4例(7.14%),甲状腺功能障碍3例(5.36%),蛋白尿4例(7.14%),疲劳4例(7.14%),口腔黏膜炎3例(5.36%),不良反应总发生23例(41.07%);
对照组患者发生高血压5例(8.93%),肝肾功能障碍5例(8.93%),甲状腺功能障碍4例(7.14%),蛋白尿4例(7.14%),疲劳4例(7.14%),口腔黏膜炎2例(3.57%),不良反应总发生24例(42.86%)。两组患者不良反应发生率经比较,差异无统计学意义(χ2=0.037,P>0.05)。
非小细胞肺癌主要是由吸烟、遗传基因、饮食等因素导致肺泡上皮、支气管黏膜上皮发生恶性增殖的一种疾病。近几年,随着环境恶化、人们不良生活习惯增多,该疾病发病率呈逐年升高趋势,且若患者治疗不及时,则易严重降低患者生活质量,不利于预后。常规单药化疗主要是通过抑制肿瘤细胞增殖以缓解患者的病情,但其在应用中效果有待进一步提高[7]。
安罗替尼作为多靶点、小分子抗癌药物,其可通过抑制机体内血管相关因子的激活,阻碍其下游信号通路,阻断内皮细胞增殖、迁移及管腔的形成,进而提高抑制肿瘤的治疗效果,延长生命时间,提高患者的生活质量[8]。同时,安罗替尼在应用中引起的不良反应相对可恢复、可控,具有较高的安全性。本研究结果显示,治疗后试验组患者DCR与对照组相比,处于更高水平;
治疗后试验组患者咳嗽、手足刺痛、气促、脱发、口腔疼痛、胸痛、吞咽困难诸项评分与对照组相比,处于更低水平;
治疗期间,两组患者不良反应发生率经比较,未见显著差异,表明安罗替尼治疗非小细胞肺癌,可提高生活质量,缓解患者的临床症状,提高临床疗效,且安全性高,与冯媛媛等[9]研究结果基本一致。VGEF作为血管内皮生长因子,可提高血管通透性,加快血管内皮细胞迁移、增殖,进而促进肿瘤增长,故其水平升高可提示患者病情恶化;
CEA、CYFRA21-1作为肿瘤标志物,可用于反映机体肿瘤病情进展情况,故其水平升高可提示患者肿瘤生长,病情加重。安罗替尼的主要作用靶点为血管内皮生长因子受体、血小板衍生生长因子受体等激酶,可通过其发挥抑制肿瘤血管形成的作用,进而抑制肿瘤生长,降低血清VGEF、CEA、CYFRA21-1水平。本研究结果显示,治疗后试验组患者血清VGEF、CEA、CYFRA21-1水平与对照组相比,处于更低水平,表明安罗替尼治疗非小细胞肺癌,可显著降低患者血清VGEF、CEA、CYFRA21-1水平,抑制肿瘤生长。
综上所述,安罗替尼治疗非小细胞肺癌,可有利于缓解患者的临床症状,降低血清VGEF、CEA、CYFRA21-1水平,改善患者生活质量,且安全可靠,能够获得理想收益,值得临床后期应用。
猜你喜欢 安罗肺癌血清 文献报道安罗替尼不良反应分析*医药导报(2022年7期)2022-08-12HOXA10基因敲低对非小细胞肺癌安罗替尼敏感性的影响中国医科大学学报(2022年6期)2022-06-24对比增强磁敏感加权成像对肺癌脑转移瘤检出的研究中国临床医学影像杂志(2022年2期)2022-05-25氩氦刀冷冻治疗肺癌80例的临床观察中国药学药品知识仓库(2022年1期)2022-03-23小分子酪氨酸激酶抑制剂安罗替尼在肺癌治疗中的应用研究进展新乡医学院学报(2021年10期)2021-11-30血清免疫球蛋白测定的临床意义中老年保健(2021年3期)2021-08-22长链非编码RNA APTR、HEIH、FAS-ASA1、FAM83H-AS1、DICER1-AS1、PR-lncRNA在肺癌中的表达昆明医科大学学报(2021年4期)2021-07-23PD-1抑制剂逆转安罗替尼获得性耐药2例报道中国现代医生(2021年5期)2021-04-02Meigs综合征伴血清CA-125水平升高1例天津医科大学学报(2021年2期)2021-03-29慢性肾脏病患者血清HIF-1α的表达及临床意义昆明医科大学学报(2021年1期)2021-02-07