初诊帕金森病患者的偏侧化研究
张荣桂 华 平 于翠玉 刘卫国
南京医科大学附属脑科医院,江苏 南京 210096
通信作者:刘卫国
帕金森病(Parkinson’s disease,PD)是全球第二大神经退行性病变,主要表现为运动迟缓、震颤、僵直等运动症状以及嗅觉减退、便秘、睡眠障碍等非运动症状[1-2]。偏侧或不对称起病是PD 显著的临床特征[3],脑影像及神经病理的相关研究也证实PD 的不对称性[4]。2015 年国际运动障碍协会(Movement Disorder Society,MDS)提出运动症状起病的偏侧化是帕金森病诊断的支持证据,而对称起病归为诊断帕金森病的“警示征”[5]。有研究表明,PD 患者的非运动症状与运动症状偏侧起病存在相关性,但目前研究较少[6-7]。本研究以初诊未服药的PD 患者为研究对象,探讨偏侧起病PD 患者间的运动、非运动症状的差异及相关影响因素。
1.1 研究对象收集2017-11—2019-09 南京医科大学附属脑科医院神经内科门诊就诊的178 例初诊未服药的帕金森病患者,其中男88例,女90例,均为右利手,所有受试者均由2名以上神经专科医生体格检查,本研究患者均知情同意,并签署知情同意书。
1.1.1 初诊PD 入组标准:(1)诊断符合2015 年MDS提出的PD 诊断标准[5];
(2)首次就诊,未服用抗帕金森病药物。
1.1.2 初诊PD 排除标准:(1)药物、脑血管病、中枢神经系统感染等引起的帕金森综合征或帕金森叠加综合征;
(2)已服药的PD 患者;
(3)不能配合量表评估;
(4)合并严重的心、肝、肾等慢性疾病。
1.2 研究方法
1.2.1 收集临床资料:收集患者的性别、年龄、发病年龄及病程等一般资料。采用统一帕金森评估量表(unified Parkinson’s disease rating scale,UPDRS)评估患者运动症状,非运动症状问卷筛查表(non-motor symptoms questionnaire,NMS Quest)评估患者非运动症状;
简易智能评估量表(mini-mental state examination,MMSE)和蒙特利尔认知评估量表(Montreal cognitive assessment,MoCA)评估患者认知功能;
汉密尔顿抑郁量表(Hamilton depression rating scale,HAMD)和 汉 密 尔 顿 焦 虑 量 表(Hamilton anxiety rating scale,HAMA)评估患者情绪状态,帕金森病患者睡眠量表(Parkinson’s disease sleep scale,PDSS)评估患者睡眠情况。
1.2.2 初诊PD 患者偏侧化分组:追溯病史,并将UPDRS III 的第20~26 项的右侧震颤、僵直、运动迟缓总分减去左侧总分,差值>0 定义为右侧起病(right-onset Parkinson’s disease,R-PD),差值<0定义为左侧起病(left-onset Parkinson’s disease,L-PD),排除差值等于0 或自述双侧同时起病的患者;
此外,本研究招募的均为右利手,故R-PD 也为优势侧起病(dominant side,DS-PD),L-PR 也为非优势侧起病(non-dominant side,NDS-PD),最终纳入169 例初诊PD患者。
1.2.3 亚型分型:根据UPDRS-Ⅱ和Ⅲ计算平均震颤评分和姿势步态异常评分,震颤评分项包括UPDRS-Ⅱ第16 项及UPDRS-Ⅲ第20~21 项,姿势步态异常评分包括UPDRS-Ⅱ第13~15 项及UPDRS-Ⅲ第29~30项。震颤评分均值与姿势步态异常评分均值的比值>1.5,定义为震颤为主型(tremor dominant,TD);
均值比值<1.0,定义为姿势不稳/步态障碍型(postural instability/gait difficulty,PIGD),均值比值介于1.0~1.5,定义为不确定型(indeterminate)[8]。
1.3 统计学方法应用SPSS 26.0 统计软件进行统计学分析,符合正态分布的计量资料用均数±标准差(±s)表示,两样本间的比较采用独立样本t检验;
非正态分布的计量资料用中位数(四分位数间距)[M(P25,P75)]表示,两样本间的比较采用Mann-Whitney U 检验;
计数资料比较采用卡方检验;
采用二元Logistic 回归进行PD 患者偏侧起病影响因素分析,P<0.05为差异有统计学意义。
2.1 2组人口学资料及运动症状比较最终纳入的169 例初诊PD 患者,男82 例,女87 例;
DS-PD 组86例,年龄(59.74±7.81)岁;
NDS-PD 组83 例,年龄(61.04±11.44)岁;
NDS-PD 组UPDRS-Ⅲ评分、H-Y 分期高于DS-PD组,2组比较差异均有统计学意义(P<0.05),2 组间性别、年龄、发病年龄、病程、亚型占比差异均无统计学意义(P>0.05),见表1。
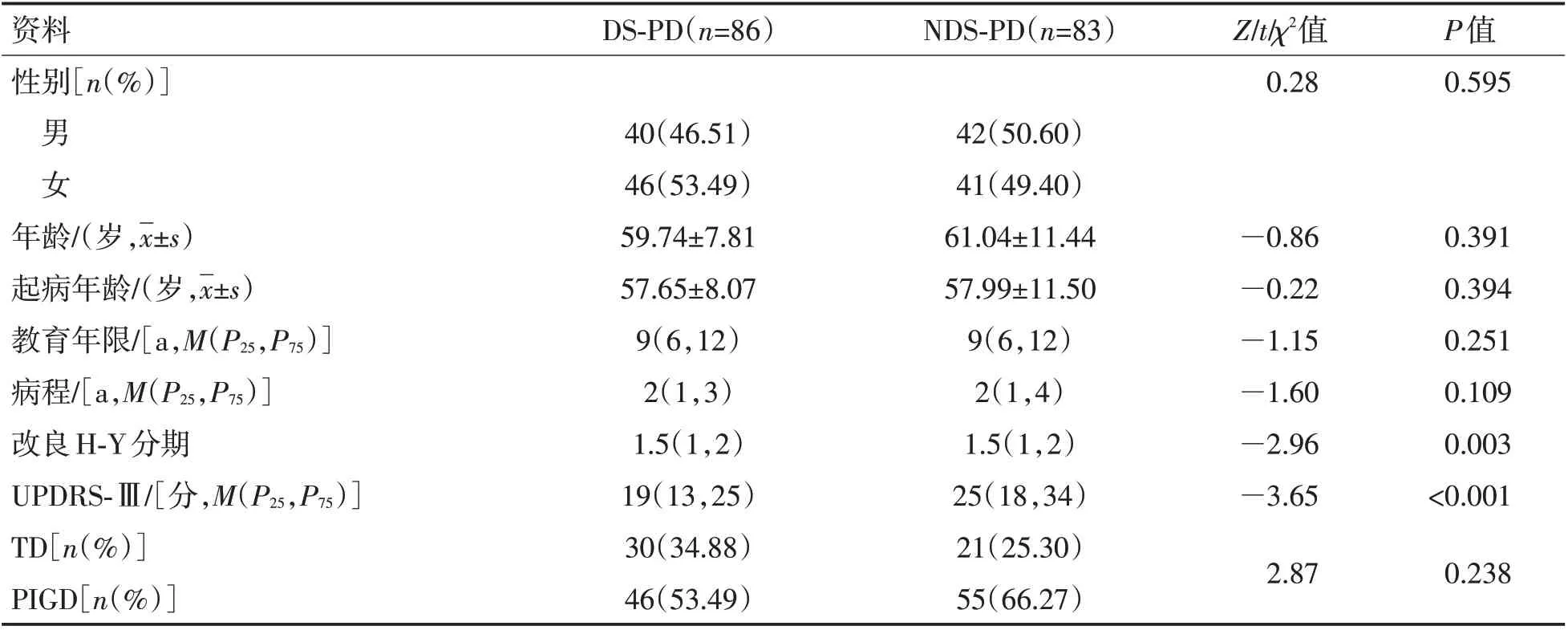
表1 2组患者社会人口学资料及运动症状比较Table 1 Comparison of demographic analysis and motor symptoms between two groups
2.2 2 组患者非运动症状比较NDS-PD 组NMS Quest总分高于DS-PD组,2组比较差异有统计学意义(P<0.05),2 组MMSE、MoCA、HAMA、HAMD、PDSS总分比较差异均无统计学意义(P>0.05),见表2。

表2 DS-PD组与NDS-PD组非运动症状比较[分,M(P25,P75)]Table 2 Comparison of non-motor symptoms between two groups [scores,M(P25,P75)]
2.3 影响偏侧起病的相关因素将是否优势侧起病为因变量,将起病年龄、性别、教育程度、MoCA、HAMD、HAMA、PDSS、NMS Quest 评分为协变量进行多因素二元Logistic 回归分析,结果显示,女性(OR=2.27,95% CI 1.145~4.524)及NMS Quest 评 分 高(OR=1.189,95% CI 1.058~1.337)是PD 患者非优势侧起病的危险因素。见表3。

表3 偏侧起病相关因素的二元Logistic回归分析Table 3 Binary Logistic regression analysis of factors related to laterality onset
偏侧化起病是帕金森病的显著临床特征,但目前对偏侧化的定义尚不明确[9]。既往对帕金森偏侧化的研究主要以非初诊PD患者为研究对象,探讨偏侧化起病的临床、影像学等特征及影响因素,考虑到药物对PD 患者运动、非运动症状的影响[10],故本研究以初诊未服药的PD患者为研究对象,避免药物对临床资料的干扰。本研究显示,DS-PD 组与NDS-PD组的人口学资料,如年龄、起病年龄、教育程度、病程、性别等差异均无统计学意义。
PD患者运动症状的偏侧化提示黑质-多巴胺能神经元的不对称丢失[11],优势侧或非优势起病与疾病的严重程度、进展是否相关目前还存在争议。HAM等[9]研究发现,优势侧较非优势侧起病的PD 患者运动症状更轻微,此外,CUBO 等[7]对652 例PD 患者进行的运动偏侧化对临床表现与生活质量影响的多中心研究发现,非优势侧起病的PD患者也表现出更严重的运动障碍。本研究中NDS-PD 患者运动缺陷更为严重,此结果与上述研究一致,可能机制如下:(1)优势半球基底节区的多巴胺能活性更高,随着多巴能神经元退行性病变,具有更强的代偿能力[12];
(2)优势半球M1区神经纤维网络更为丰富,且仅在非优势半球观察到运动相关皮质变薄的现象[13-15];
(3)躯体的活动能够增强突触可塑性及神经发生,并减少神经炎症反应,从而改善运动症状[16-17];
(4)非优势侧起病患者可能更迟意识到其非惯用手的运动缺陷,导致延迟诊断和症状表现更为严重。在相等程度神经退行性病变中,优势侧起病的PD患者具有更强的调节能力及适应性,运动障碍表现得更为轻微。
PD患者非运动症状是否存在偏侧化表现,目前仍存在争议。本研究对2 组非运动症状比较中,除NDS-PD 组NMS Quest 评分较高外,其余项如MoCA、HAMA、HAMD、PDSS 评分等差异均无统计学意义,提示认知、焦虑、抑郁等非运动症状与偏侧化起病无明显相关性,但NDS-PD 组NMS Quest 评分更高,反映优势侧起病组患者非运动症状受累更为明显,与ESTHER 等[7,18]的研究结果一致,且与上述运动症状偏侧化结果一致,提示优势侧起病的PD患者非运动症状也具有更强的代偿、适应能力。
既往研究报道,环境、遗传、起病年龄、运动等可能是PD患者偏侧化起病的影响因素[19],但目前尚存在争议。本研究中二元Logistic回归分析显示,性别及NMS Quest评分可能是PD患者偏侧化起病的影响因素,起病年龄无显著影响。国内外关于性别是否影响PD 患者偏侧起病的研究较少,目前尚无定论,UITTI 等[20]未发现性别与偏侧起病存在相关性,但BENTIVOGLIO 等[21]研究发现,左侧起病的PD 患者男性多见,性别可能是PD患者偏侧化起病的影响因素,然而此结果未进行矫正,且可能存在入组偏倚,因此,性别是否影响PD起病的偏侧化,还需多中心、多种族并结合影像、遗传等因素进行综合分析。此外,非运动症状,如嗅觉减退[22-42]、便秘、抑郁等[43-52]常出现在运动症状前。本研究显示,NMS Quest评分为运动症状非优势侧起病的危险因素,且在相关分析中,NDS-PD 组NMS Quest 评分显著高于DS-PD 组,仍可能提示优势大脑半球存在的神经代偿、适应机制。
本研究存在以下不足:(1)本研究为单中心、横断面研究;
(2)缺乏神经影像学、生物标志物等资料对偏侧化起病差异性及影响因素的综合分析。性别可能是PD患者偏侧化起病的影响因素,非优势半球起病的PD 患者运动及非运动症状受累更严重,因此,对非优势侧起病的PD 患者,在疾病早期需更注重制定规范的个体化治疗方案。
